复合肥用多了会造成土壤酸化吗?
土壤酸化是土壤溶液中氢离子H+的积累,土壤pH值下降,衡量指标是土壤酸度。土壤酸化对作物生长的最大伤害不是来自于H+离子,而是源于低pH下铝离子释放到土壤中。当pH值降低到5.5以下时,铝离子和锰离子的浓度增加,可能达到对植物产生毒性的浓度,从而干扰根系的生长和功能,并限制植物对营养物质的吸收。农业系统中使用的化肥是土壤pH变化的主要驱动因素。
氮肥氮肥的主要形式有尿素(CO(NH2)2)、磷酸二氢铵(NH4H2PO4)、磷酸氢二铵((NH4)2HPO4)、硝酸铵(NH4 NO3)、硫酸铵((NH4)2SO4)。
氨氮NH4:氮肥在土壤pH酸化中的关键分子是氨氮。随着化肥中氨氮的硝化作用,细菌将铵转化为硝酸盐,释放的氢离子H+会增加土壤酸度。每硝化一个铵分子会产生两个H+离子,从而降低pH值。
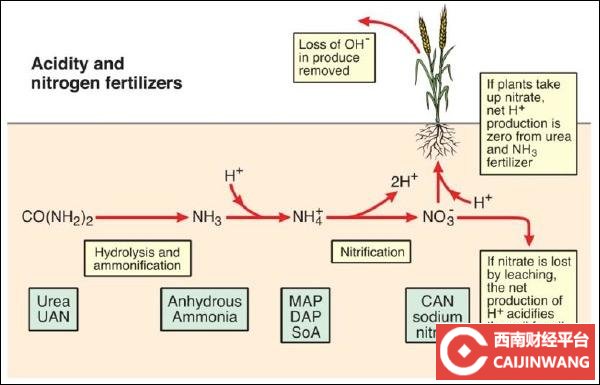
尿素:尿素只能轻微酸化土壤。当尿素被添加到土壤中时,反应形成碳酸氢盐和氨氮。然后,碳酸氢盐与土壤溶液中的H+离子发生反应,降低酸度,但当氨氮被硝化时,酸度又会增加,因此总的净效应是几乎没有影响。
硝氮
硝酸钙和硝酸钾不会使土壤酸化,硝氮肥料没有酸化土壤的潜力,实际上可以增加土壤pH值,因为植物在吸收硝酸盐时吸收了一个H+离子或排泄一个OH-。
磷肥主要形式是磷酸二氢铵(NH4H2PO4)、磷酸氢二铵((NH4)2HPO4)。磷酸二氢铵以H2PO4-离子的形式向土壤中添加磷,高pH下,H2PO4离子中H+离子的解离会产生一定的酸性,可使pH大于7.2的土壤酸化,但对酸性土壤的pH没有影响。
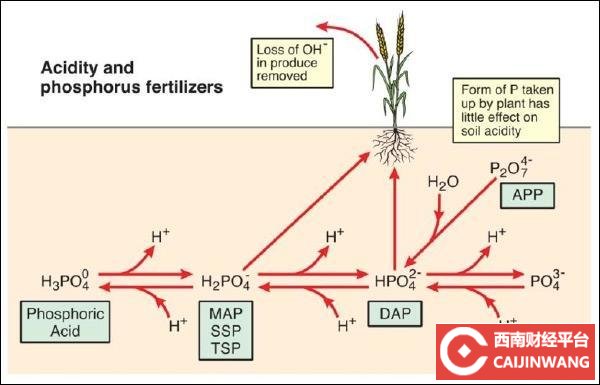
磷酸氢二铵中P的形式为HPO42-,当土壤pH小于7.0时,磷酸盐离子会与游离氢离子发生反应生成H2PO4-,并在一定程度上降低酸度,但对pH为大于7.2的土壤没有影响。

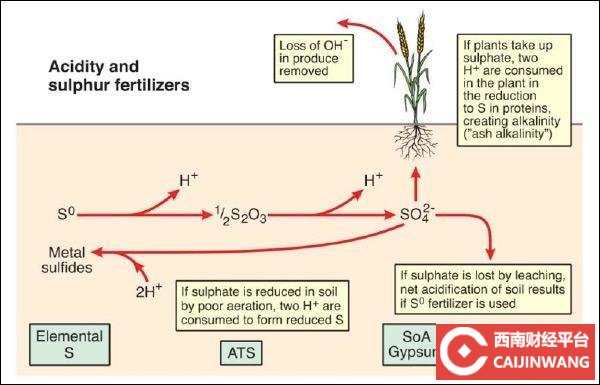
硫
硫添加到土壤会通过释放H +离子增加土壤酸度,每1分子硫将生成两个H +离子,但是与施肥添加到土壤的大量的氮肥相比,硫的量相对较低,对土壤pH影响较小。
- 发表于 2022-01-13 16:34
- 阅读 ( )
- 分类:科学